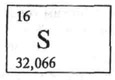-
В закладки
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.сера
се́ра, -ы -
В закладки
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.Сера
СЕРА (лат. Sulfur) - S, химический элемент VI группы периодической системы Менделеева, атомный номер 16, атомная масса 32,066. Желтые кристаллы. Устойчива в двух модификациях - ромбической (плотность 2,07 г/см³, tпл 112,8 .С) и моноклинной (плотность 1,96 г/см³, tпл 119,0 .С). В воде нерастворима. На воздухе устойчива; при горении дает SO2, с металлами образует сульфиды. В природе - самородная сера, сульфиды, сульфаты. Серу выплавляют из самородных руд; получают также окислением кислородом воздуха сероводорода, содержащегося в природном, нефтяном, коксовом газах, и др. методами. Ок. 50% серы идет на получение серной кислоты, 25% - на получение сульфитов (используются в бумажной промы …
Далее -
В закладки
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.сера
-ы, ж.1.Химический элемент, легко воспламеняющееся вещество желтого цвета (применяется в промышленности, военном деле, сельском хозяйстве, медицине).2.Желтое жирное вещество, образующееся на стенках ушного канала.3. обл.Смола, выделяющаяся из хвойных деревьев.Руки у Матвея Сибиряка обыкновенные, жилистые и рябоватые, только не от оспы, как лицо, а от несмываемых пятен еловой и сосновой серы. В. Смирнов, Открытие мира. -
В закладки
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.Сера
ж. 1.Химический элемент, легко воспламеняющееся вещество желтого или сероватого цвета.2. разг.Жирное густое вещество желтого цвета, образующееся на стенках ушного канала.3. местн.Смола, выделяющаяся из хвойных деревьев. -
В закладки
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.Сера
серы, мн. нет, ж. 1. Металлоид, легко воспламеняющееся вещество желтоватого или сероватого цвета, применяемое в медицине и технике. 2. Жирное густое вещество желтого цвета, образующееся на стенках ушного канала (разг.). Скопление серы. -
В закладки
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.СЕРА
СЕ́РА, -ы, жен.1. Химический элемент жёлтое горючее вещество, применяемое в технике и медицине.2. Жёлтое жирное вещество, образующееся в ушном канале.| прил. серный, -ая, -ое. -
В закладки
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.СЕРА
жен. одно из простых (несложных, неразлагаемых) веществ, плавкое и сильно горючее ископаемое вулканического рожденья; как товар, зовут ее: сера горючая. Порох делается из селитры и серы, с углем. Черенковая сера, отлитая палочками.| Сера, серка, вост. и сиб. мастика южн. топленая смола лиственицы, которую жуют, заобычай, как лакомство, и чтоб зубы белели. Льнет, как сера (смола) к сучку (к стене).| Мылистое вещество (щелочно-жирное), отделяемое природой в ушном проходе. Нередко люди глохнут от скопа серы, заткнувшей ухо пробкою. Сера в ушах кипит, нос залегает, к ненастью. Серный, к сере относящийся. Серный цвет, дух, вкус. Серный цвет, мелкий порошок, от сухой перегонки серы. Серное молоко,…
Далее -
В закладки
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.Сера
се́ра укр. сíра, др.-русск. сѣра, сербск.-цслав. сѣра θεῖον, болг. ся́ра, чеш. síra, слвц. sirkа "спичка", польск. siara, siarka. Лит. sierà "сера", лтш. sę̃rs – то же заимств. из вост.-слав. (М.–Э. 3, 830). Праслав. *sěrа не может быть родственно се́рый, вопреки Брюкнеру (487), Шрадеру–Нерингу (2, 359), Младенову (626), потому что в этом случае ожидалось бы зап.-слав. š. Неясно отношение *sěrа к др.-русск. цѣрь "сера" (Пов. врем. лет под 946 г.), которое пытался связать с ним уже Миклошич (Мi. ЕW 295). Колебания начала слова можно было бы объяснить заимствованием. Не внушает доверия предположение о родстве *sěrа со ср.-в.-н. hаrе, hаrеwеr "терпкий, горький" (М.–Э. 3, 830) или с др.-и …
Далее -
В закладки
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.Сера
(лат. Sulfur), хим. элемент VI гр. периодич. системы. Жёлтые кристаллы. Устойчива в двух модификациях - ромбической (плотн. 2,07 г/см3, tпл 112,8 °С) и моноклинной (плотн. 1,96 г/см3, tпл 119 °С). В воде нерастворима. На воздухе устойчива; при горении даёт SO2, с металлами образует сульфиды. В природе - самородная С., сульфиды, сульфаты. С. выплавляют из самородных руд; получают также окислением кислородом воздуха сероводорода, содержащегося в природном, нефт., коксовом газах, и др. методами. Ок. 50% С. идёт на получение серной кислоты, 25% - на получение сульфитов (используются в бум. пром-сти), остальная - для борьбы с болезнями р-ний, вулканизации, синтеза красителей, произ-ва спичек и др
…
Далее -
В закладки
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.Сера
(Sulfur) S, хим. элемент VI гр. периодич. системы, ат. н. 16, ат. м. 32,066; относится к халькогенам. Природная С. состоит из четырех изотопов: 32S (95,084%), 33S(0,74%), 34S(4,16%), 36S(0,016%). Поперечное сечение захвата тепловых нейтронов для прир. смеси изотопов 0,52
-
В закладки
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.Сера
(Sulfur; S) химический элемент VI группы периодической системы Д. И. Менделеева; атомный номер 16, атомная масса 32,06; твердое кристаллическое вещество желтого цвета, нерастворимое в воде; используется при изготовлении некоторых лекарственных средств; соединения С. широко распространены в живой природе. -
В закладки
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.Сера
(S), химический элемент, твердое, нерастворяющееся в воде, кристаллическое вещество желтого цвета. -
В закладки
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.Сера
хим. элемент, символ S (лат. Sulfur), ат. н. 16, ат. м. 32,066. С. - твёрдое хрупкое в-во жёлтсго цвета, имеет аллотропные модификации. Наиболее устойчивы и изучены ромбическая С. (а-S) С плотн. 2070 кг/м3, устойчивая ниже 95,5 о С, и моноклинная С. (бета-S) c плотн. 1960 кг/м3, устойчивая от 95,6 до 119,3 °С (tпл). В природе С. встречается как в свободном состоянии (самородная С.), так и гл. обр. в виде соединений - сульфидов (пирит, или серный колчедан; халькопирит, или медный колчедан; сфалерит, или цинковая обманка, и др.) и сульфатов (гипс, барит, глауберова соль и др.). Элементарную С. добывают из самородных руд; её получают также окислением сероводорода H2S и восстановлением серного а
…
Далее -
В закладки
 В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.
В закладки будет добавлено толкование к данному слову в данном словаре. Закладки сохраняются на Вашем компьютере в cookie. Если Ваш браузер не поддерживает cookie или такая возможность отключена, то сохранение закладок будет не возможно.Сера
В мифологии ирландских кельтов Сера - отец Парталона. Согласно некоторым источникам, именно Сера, а не Парталон был мужем Дилгнейд.